近期,药学院李志裕教授/卞金磊教授课题组联合工学院顾月清教授/马祎副教授课题组在医学学科顶尖期刊Acta Pharmaceutica Sinica B发表广谱谷氨酰胺代谢拮抗剂光敏前药最新研究成果:Tumor-targeted metabolic inhibitor prodrug labelled with cyanine dyes enhances immunoprevention of lung cancer。药学院硕士研究生李文、沈晨,博士研究生黄佳丽为本论文的共同第一作者,中国药科大学为本文的唯一通讯单位。
“谷氨酰胺成瘾”是肿瘤代谢重编程过程的重要部分,是癌细胞生长的显著特征。因此,发现能广泛抑制谷氨酰胺代谢的拮抗剂,已变得至关重要,成为当前抗癌药物研发的一大热点。其中,天然化合物DON(6 Diazo-5-oxo L norleucine, 6-重氮-5-氧代-L-正亮氨酸)是目前研究最为广泛的谷氨酰胺拮抗剂,最高推进到临床II期研究。然而,临床试验揭示了其治疗窗口狭窄,以及明显的胃肠道副作用。这主要是因为正常胃肠道细胞同样依赖谷氨酰胺,导致DON在胃肠组织中大量积累,干扰了正常的谷氨酰胺代谢,对健康组织造成伤害。
DON的毒性源自药效作用机理,常规的结构修饰无法在保持药效的情况下实现减毒作用,只有通过引入具有特异性识别功能的靶向基团,设计合成肿瘤靶向性DON前药,选择性地将药物递送至病灶部位,才能降低对正常细胞、组织和器官的毒性作用,从而提高其治疗窗。如何利用肿瘤与正常细胞微环境的差异,通过定点特异性激活从而达到药物的肿瘤靶向释放,是DON作为谷氨酰胺代谢拮抗剂在临床进一步开发的关键与难点。
光触发前药以其非侵入性以及可操控性,在肿瘤治疗领域展现出巨大的应用前景。而近红外光也因其能量低、对组织损伤小、高组织渗透性等优势成为光疗的首选光源。本研究设计合成所得的最优化合物结构为DON-TK-BM3——将异丙基保护的DON 通过ROS响应型硫缩酮链(TK)与花菁染料进行结合。在近红外光的照射下,花菁染料产生单线态氧使TK链发生断裂,释放出DON药物以及花菁探针。这一设计不仅实现了DON在肿瘤组织中的精确靶向积累,优化了药物的释放机制(“如何释放”),还通过药物释放前后的结构变化,改变了荧光光谱,提供了释放时间(“何时释放”)的精确信息。体内活性研究进一步证明,DON-TK-BM3不仅实施了一种光动力治疗策略,抑制了肿瘤细胞的三羧酸循环(TCA),扭转了肿瘤的免疫抑制微环境,还显著增强了抗肿瘤效果,同时大幅降低了药物的副作用。这些研究结果不仅表明该前药技术在临床应用上的广阔潜力,也为针对癌症代谢靶点的药物开发提供了新的策略方向。
该研究工作受到了国家自然科学基金面上项目、江苏省自然科学基金优秀青年基金和中国药科大学“双一流”学科创新团队、国家高层次青年人才计划、中国药科大学兴药学者计划等资助。
文章链接:https://www.sciencedirect.com/science/article/pii/S2211383523004173?via%3Dihub
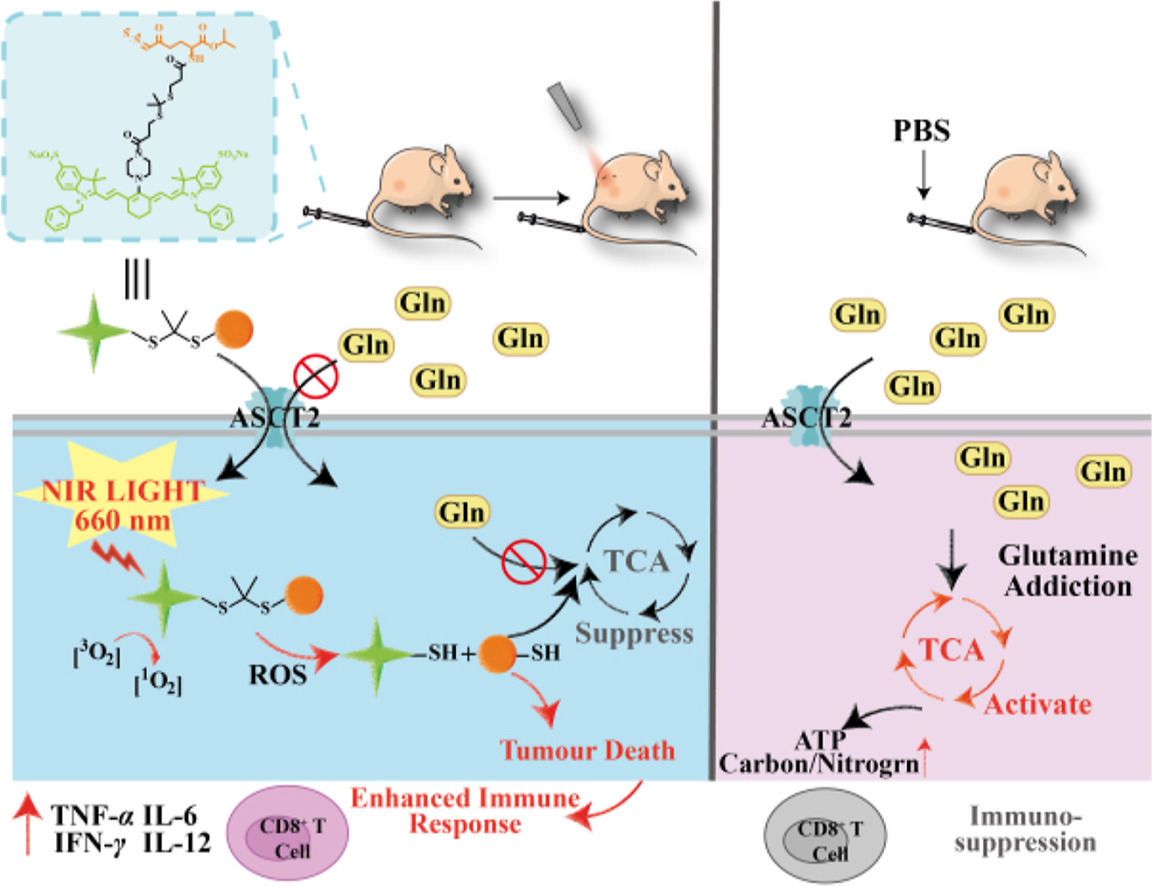
示意图
(供稿单位:药学院,撰写人:刘华)


