近日,药学院姜虎林教授团队在学科顶尖期刊Acta Pharmaceutica Sinica B、Advanced Science及Chinese Chemical Letters相继发表胰腺纤维化治疗的系列最新研究成果。
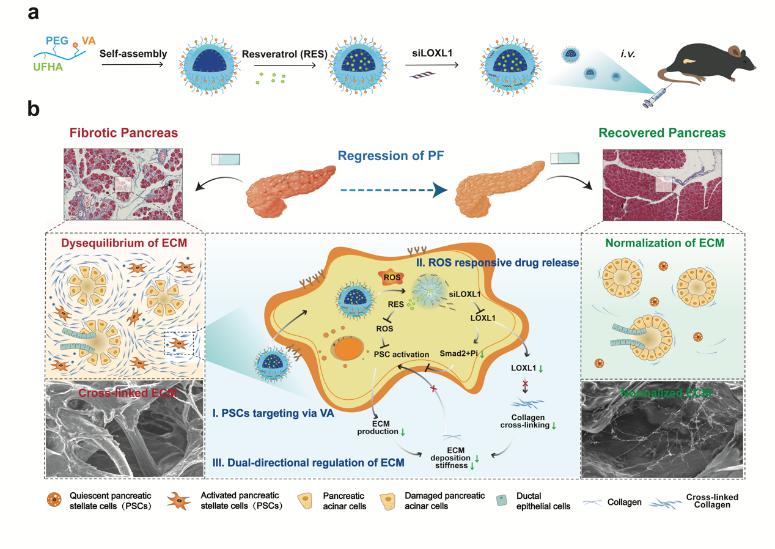
胰腺纤维化主要表现为胰腺星状细胞(PSC)持续激活,引起胶原过度沉积导致的细胞外基质(ECM)稳态失衡。而且过度沉积的胶原会形成病理屏障,严重阻碍药物的有效递送。针对上述问题,姜虎林教授团队前期已设计并制备胶原结合肽和胶原酶I共修饰的双重载药脂质体(命名为AT-CC),用于胰腺纤维化治疗(Biomaterials 2023, 292, 121945)。在此基础上,团队进一步构建PSC靶向调控制剂,清除积聚的ROS,抑制PSC激活,同时抑制胶原交联,促进ECM降解,协同重塑基质与微环境稳态平衡。该研究成果以“Reactive oxygen species-responsive nanoparticles toward extracellular matrix normalization for pancreatic fibrosis regression”为题发表在Advanced Science上,东南大学医学院祁靓博士和中国药科大学段博文博士生为论文共同第一作者,中国药科大学药学院姜虎林教授、美国加州大学Stephen J. Pandol教授和东南大学附属中大医院李玲教授为本文共同通讯作者。
全文链接:https://doi.org/10.1002/advs.202401254
示意图
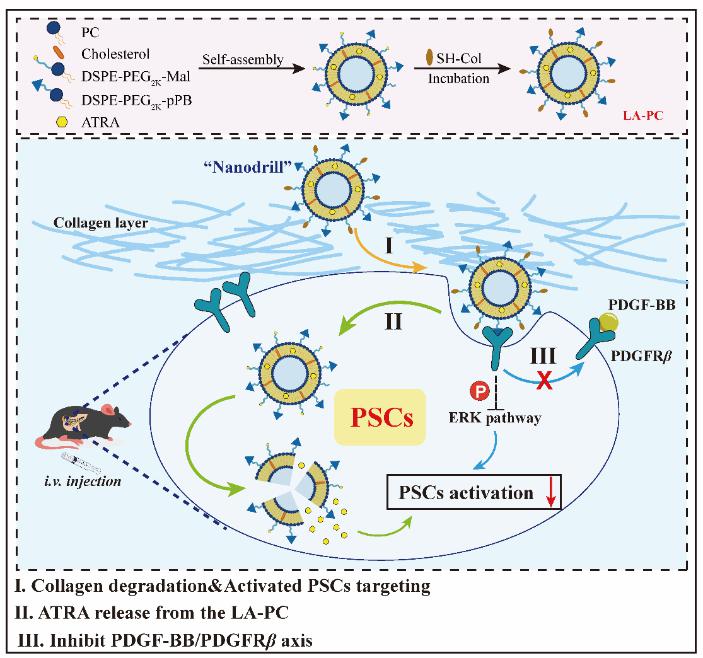
PSC的活化在CP的始动和演进过程中均发挥了重要作用,其分泌的致密ECM严重阻碍了治疗药物向靶部位胰腺的深层递送,大大削弱了药物的抗胰腺纤维化治疗效果。针对这一问题,该研究团队通过在脂质体表面负载胶原酶I和PSC靶向肽(pPB肽)设计了一种全新的PSC靶向调控平台(命名为LA-PC),胶原酶I能够有效分解CP胰腺中致密的ECM层,实现LA-PC的胰腺组织深层分布。此外,LA-PC表面修饰的pPB肽与激活的PSC表面血小板衍生生长因子受体β(PDGFRβ)相结合,增加PSC对药物的有效摄取。这一有效结合还能够抑制血小板衍生生长因子B(PDGF-BB)对PDGFRβ的激活,进而抑制其下游MAPK通路,抑制PSC的活化,有效治疗胰腺纤维化。该研究成果以“A PDGFRβ-targeting nanodrill system for pancreatic fibrosis therapy”为题发表在Chinese Chemical Letters上,论文第一作者为中国药科大学药学院韩涵博士后和陈比特硕士生,药学院姜虎林教授和邢磊副教授为本文共同通讯作者。
全文链接:https://doi.org/10.1016/j.cclet.2024.109583
示意图
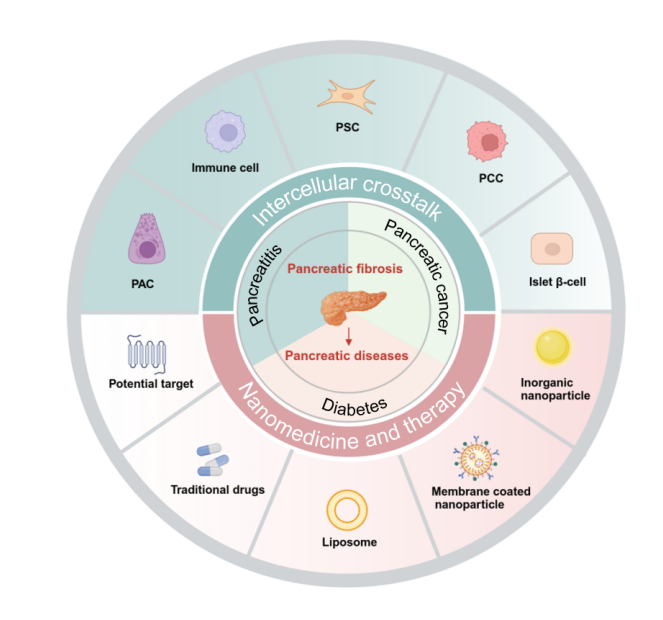
不同疾病背景下,纤维化病理微环境中与PSC相互作用的细胞机制不同。基于前期的工作基础,本团队系统总结纤维化在三种常见胰腺内外分泌疾病(包括胰腺炎、胰腺癌和糖尿病)进展中的作用,并分析了不同疾病的纤维化微环境中错综复杂的细胞间互作机制,探讨了纳米药物在纤维化及胰腺疾病中的潜在靶点及治疗策略,为深入了解胰腺疾病中PSC介导的细胞间互作机制及基于纳米药物的精准治疗提供有价值的见解,以“Nanomedicine regulating PSC-mediated intercellular crosstalk: mechanisms and therapeutic strategies”为题发表在Acta Pharmaceutica Sinica B上,论文共同第一作者为东南大学医学院王慧博士生、祁靓博士和中国药科大学药学院韩涵博士后,东南大学附属中大医院李玲教授和中国药科大学药学院姜虎林教授为本文共同通讯作者。
全文链接:https://doi.org/10.1016/j.apsb.2024.07.007
示意图
目前姜虎林教授团队聚焦于开发多层次、全方位的抗纤维化制剂,已在肝、肺和胰腺等脏器的纤维化疾病中展现较好的治疗效果。相关研究成果获国家专利8项,并有1项肺纤维化治疗相关专利成功转化。该团队将进一步聚焦多脏器纤维化的逆转,开发纤维化治疗药物,同时积极推动研究开发向科技成果的落地转化。
以上工作获得国家自然科学基金重点国际(地区)合作研究项目和科技部重点研发计划项目以及中国药科大学多靶标天然药物全国重点实验室研究项目的资助。
(供稿单位:药学院,撰写人:刘华)


