近日,药学院李苏昕教授团队在 Cell Press细胞出版社期刊Cell Reports Medicine(IF=11.7)发表了研究论文:A dual-STING-activating nanosystem expands cancer immunotherapeutic temporal window。李苏昕教授为本文的主通讯作者,中国药科大学为第一通讯单位。
STING是肿瘤免疫治疗的明星靶点,然而STING激活后会迅速完成内质网-高尔基体-溶酶体转运,最终被降解导致免疫效应终止,作为机体自我保护的机制。因此小分子激动剂的治疗窗口期非常狭窄,难以为抗肿瘤免疫系列事件持续提供信号输出。而高剂量或频繁给药易造成免疫耗竭和系统毒性,目前多款药物在临床早期阶段停滞不前。
该研究设计了一款具有双重STING激活能力的纳米胶束制剂D-SAM,通过调控STING胞内转运与降解过程,延长下游免疫信号活化时间,放大抗肿瘤免疫疗效。其中小分子激动剂迅速激活STING,同时借助高分子载体的质子海绵效应抑制活化的STING蛋白被溶酶体降解,持续提供STING激活信号。该“刺激-锁定”模式显著促进DC的抗原交叉呈递,有效延长效应T细胞的活化与浸润时间,同时避免了T细胞的耗竭与凋亡。在结直肠癌、黑色素瘤、乳腺癌等小鼠模型中表现出显著的抑瘤效率,并能防止肿瘤的复发与转移。进一步利用肿瘤病人组织样本,考察了临床转化的适配性。
该研究揭示了STING调控肿瘤免疫微环境的时间动力学规律,提示时间节律在药物递释系统设计中的重要作用。工作得到国家重点研发计划、国家自然科学基金、江苏省自然科学基金、多靶标天然药物全国重点实验室、江苏省药物分子设计与成药性优化重点实验室等资助。
原文链接:https://doi.org/10.1016/j.xcrm.2024.101797
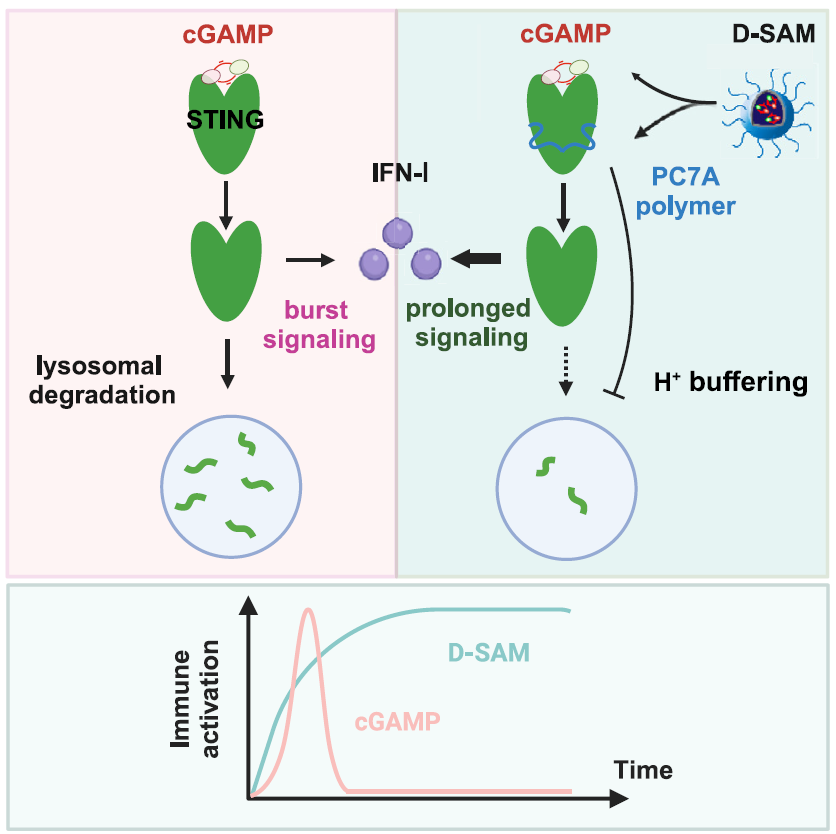
示意图
(供稿单位:药学院,撰写人:刘华)


