近日,中国药科大学药学院何玉立研究员、姚和权教授团队在国际权威期刊JOURNAL OF THE AMERICAN CHEMICAL SOCIETY在线发表题为“Nickel-Catalyzed Asymmetric Carboacylation of Alkenes via CO Transfer”的研究论文。药学院2025级博士研究生张文为第一作者,药学院姚和权教授和何玉立研究员为共同通讯作者,中国药科大学为第一通讯单位。
手性羰基结构广泛存在于天然产物和小分子药物中。据统计,近年来美国FDA批准的小分子药物中,约有四分之一含有手性羰基结构单元。尽管针对该类化合物的不对称合成已取得显著进展,但现有方法仍存在诸多局限,例如底物适用范围有限、依赖贵金属催化剂、需使用有毒一氧化碳气体,或试剂通用性不足。因此,开发高效、实用且具有广泛适用性的光学纯羰基化合物合成方法,仍具有重要意义和迫切需求。
针对上述挑战,研究团队基于“官能团转移(Functional Group Transfer)”理念,创新性地利用酰氯同时作为“碳源”和“羰基源”,在镍催化体系下实现了烯烃的不对称碳酰化反应。通过对CO“释放—再插入”过程的精确动力学调控,成功实现了区域选择性与对映选择性的协同控制,在无需外加CO气体的条件下,高效合成了一系列手性酮类化合物。
在优化反应条件下,该方法可实现最高达99% ee的优异对映选择性,并表现出良好的官能团兼容性。反应体系适用于多种酰氯、未活化烯烃及不同类型的烷基卤代物,包括一级、二级和三级卤代烃。值得注意的是,该策略可用于复杂分子及药物相关骨架的后期修饰,如丙磺舒和非诺贝特衍生物的功能化,显示出良好的应用前景。此外,所得产物还可进一步转化为手性γ-内酯等重要结构单元,为复杂活性分子的快速构建提供了新的合成工具。
本研究提出了一种合成手性羰基化合物的全新通用策略,不仅显著拓展了不对称催化反应的研究边界,也为药物分子合成及复杂分子的后期官能化提供了有力手段,同时为双功能试剂的进一步开发以及无CO参与的不对称羰基化在复杂分子合成中的应用奠定了重要基础。
以上工作得到了国家自然科学基金面上项目(NSFC22371298,NFSC22371299)和多靶标天然药物全国重点实验室自主研究课题项目(SKLNMZZ202211)的资助。
文章链接:https://pubs.acs.org/doi/10.1021/jacs.5c23037
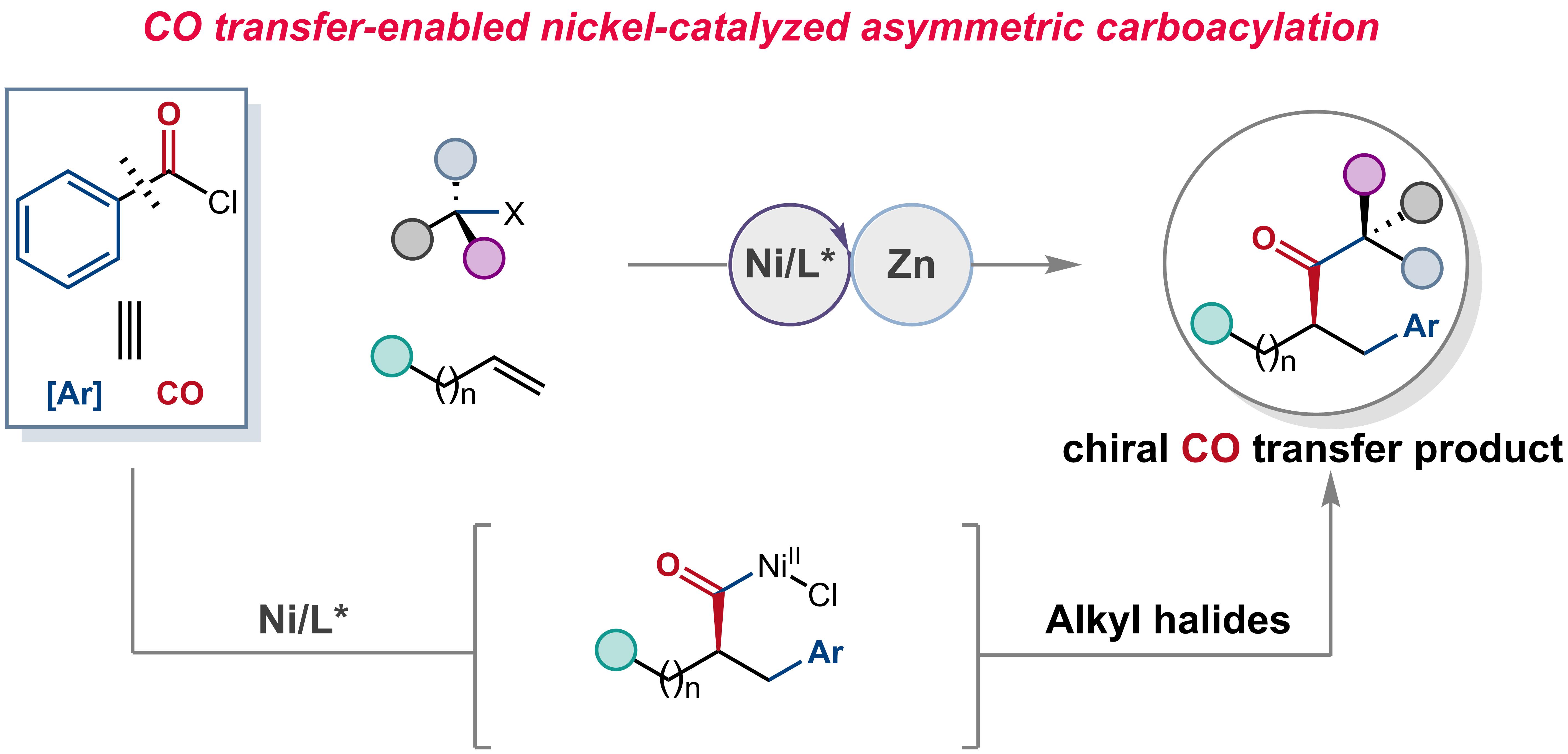
示意图
(供稿单位:药学院,撰写人:刘华)


