近日,我校药学院尹莉芳/辛晓斐/秦超团队在权威期刊Journal of the American Chemical Society上发表题为“Structure-Activity-Driven Multicompartment Lipid Nanoparticles for Synergistic mRNA and siRNA Codelivery in Acute Myeloid Leukemia”的研究论文。药学院尹莉芳教授、辛晓斐副研究员、秦超副教授和中国科学院上海高等研究院李娜研究员为本文共同通讯作者,中国药科大学2021级博士生吕一甫和2023级硕士生秦焕宇为共同第一作者,中国药科大学为第一通讯单位。
急性髓系白血病(AML)进展中,STAT3异常激活与内质网应激会削弱树突状细胞(DCs)抗原递呈,诱发T细胞耗竭与免疫逃逸,而常规脂质纳米颗粒(LNPs)因结构单一、组织分布缺乏特异性,难以在脾脏和淋巴结等免疫器官实现mRNA与siRNA的高效共递送。为此,本研究基于构效关系驱动的分子设计,引入咪唑极性头基,合成形成非层状多室结构的LNP,其中由哌嗪环与双咪唑构成M型头基的可电离脂质A3-DM/DL表现最优,可显著增强膜相互作用、细胞摄取与转染效率,实现mRNA与STAT3靶向siRNA协同递送:一方面在免疫器官髓系细胞中高效沉默STAT3并缓解内质网应激以恢复DCs功能,另一方面协同递送mRNA逆转肿瘤微环境T细胞耗竭,激活NK细胞与T细胞介导的抗白血病免疫,从而显著改善小鼠AML。总体而言,该工作为理性构建多室LNP克服异质核酸共递送瓶颈并通过重塑免疫微环境实现协同治疗提供了新策略。
原文链接:https://doi.org/10.1021/jacs.5c23209
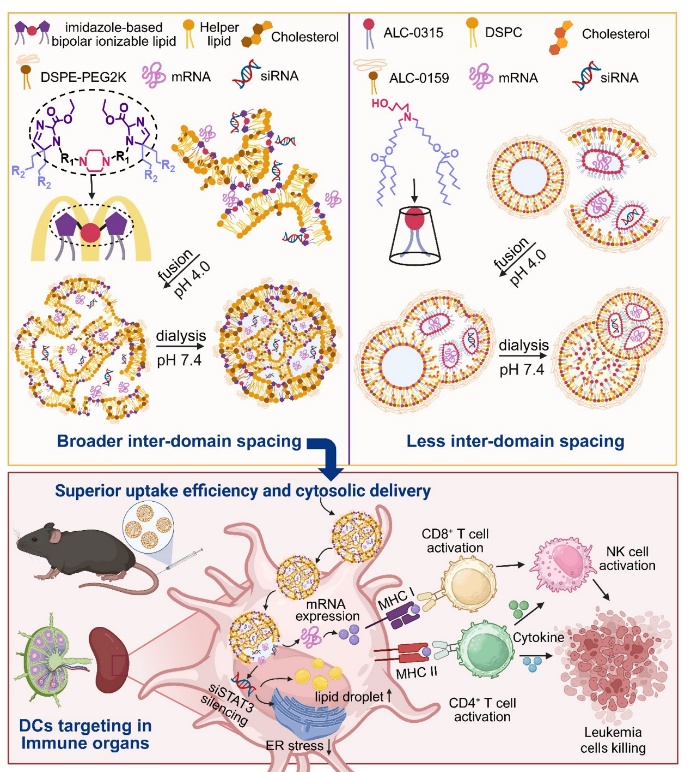
示意图
在前期口服核酸递送研究(ACS Nano, 2025)的基础上,团队进一步将LNP平台向口服给药与肠淋巴转运方向拓展,以提升给药依从性并利用淋巴吸收路径实现免疫相关组织的靶向暴露,并与韩思飞/胡罗娟团队合作在学科顶尖期刊Chemical Engineering Journal发表研究论文“In situ formation of chylomicron-incorporated lipid nanoparticles via muramyl dipeptide conjugation potentiates lymphatic transport of chemoimmunotherapeutic for leukemia therapy”,提出通过胞壁酰二肽功能化促进LNP制剂经乳糜微粒途径进入淋巴系统,从而增强对白血病治疗相关淋巴组织的递送效率与疗效。中国药科大学2022级硕士生赵鹏博、2024级博士生丁钰、2023级硕士生袁银银为共同第一作者,中国药科大学为论文第一通讯单位。
原文链接:https://doi.org/10.1016/j.cej.2026.173750
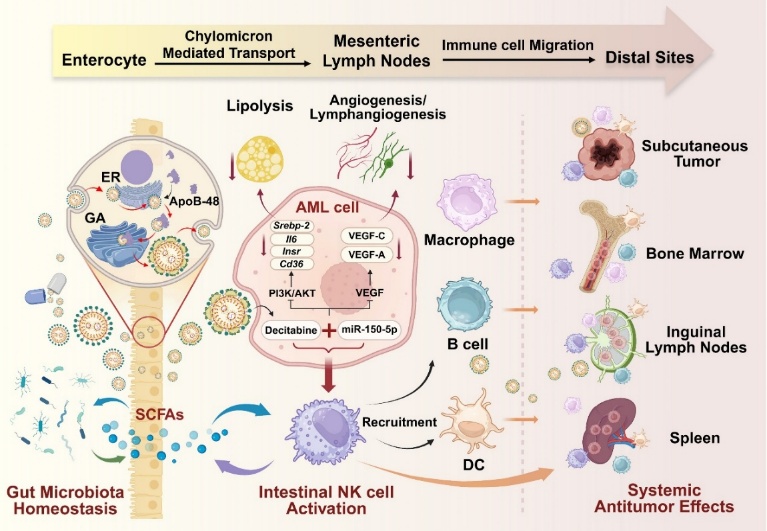
示意图
综上,这些成果从结构可编程-器官定向-给药路径升级三个维度,形成了LNP技术体系的连续推进与整体化布局,为核酸/小分子联合递送与免疫微环境重塑治疗提供了平台化证据链。
(供稿单位:药学院,撰写人:刘华)


