近日,药学院张文丽副教授团队在工学学科顶尖期刊Advanced Functional Materials发表研究论文:Eradicating Helicobacter Pylori with a Multifunctional Trojan Horse Nanoplatform Armored with β-Cyclodextrin。药学院张文丽副教授为本文的通讯作者,药学院研究生王昕秋悦、张蕾为本文共同第一作者,中国药科大学为唯一通讯单位。
幽门螺杆菌感染是一种严重威胁人类健康的疾病,传统疗法常因宿主自噬功能障碍而疗效受限。宿主导向疗法为其治疗提供了可行方案,然而,如何克服生物屏障并精准靶向感染细胞仍是该疗法临床转化的关键难题。
本研究成功构建了一种名为BPI-CD-LCR的自驱动“特洛伊木马”纳米递送系统,该系统共修饰细菌靶向肽和脲酶动力马达,其中β-环糊精在药物递送和自噬调控中发挥了多重关键作用。在递送层面,β-环糊精通过与脲酶形成动态复合物,有效保护其在胃酸环境中的活性,为纳米粒主动穿透胃黏液屏障提供持续驱动力。抵达感染部位后,该系统该系统一方面通过追踪细菌启动“特洛伊木马”机制,介导巨噬细胞的调理吞噬;另一方面,表面的β-环糊精通过提取感染巨噬细胞膜上的胆固醇,增加膜流动性,协同促进细胞摄取,实现精准靶向递送。在自噬调控层面,进入细胞后,β-环糊精联合白藜芦醇,通过促进自噬体-溶酶体融合和恢复溶酶体功能,协同重塑自噬通路,重启对胞内幽门螺杆菌的清除。
在小鼠幽门螺杆菌感染模型中,该纳米递送系统实现了胃内细菌载量的显著降低,效果较传统抗生素三联疗法提升了33倍。综上,本研究为难治性感染提供了一种基于纳米工程的递送策略,通过精准引导宿主导向疗法实现感染细胞内的按需抗菌激活,为幽门螺杆菌的根治提供了新的解决方案。
原文链接:http://doi.org/10.1002/adfm.202528258
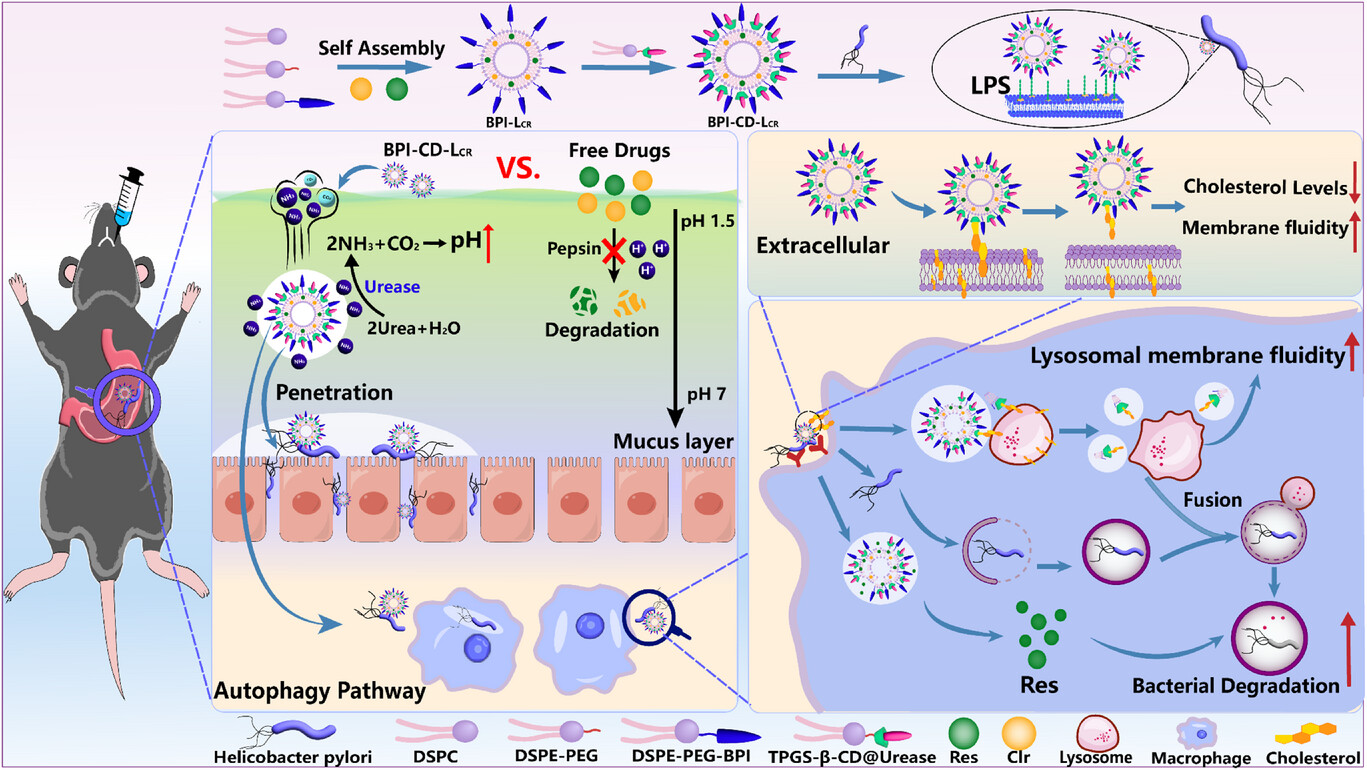
示意图
(供稿单位:药学院,撰写人:刘华)


