近日,中国药科大学药学院张文丽副教授团队与新西兰奥克兰大学Zimei Wu教授团队在工学学科一流期刊SMALL合作发表题为“A Biomimetic Micro-Nano System Maximizing ‘Active Transport and Retention’ Effect in Solid Tumors”研究论文。中国药科大学与新西兰奥克兰大学联合培养博士生杨开云为论文第一作者,张文丽副教授和Zimei Wu教授为共同通讯作者,中国药科大学和新西兰奥克兰大学为共同通讯单位。
传统抗肿瘤纳米药物依赖EPR效应的被动靶向存在显著局限性,在不同肿瘤类型中表现不佳且异质性高。近年来,“主动转运与滞留”(ATR)策略通过促进纳米载体跨内皮转运,展现出更好的肿瘤深部递送潜力。然而,ATR仍面临靶向效率不足、药物外排和细胞内滞留率低等挑战。此外,网状内皮系统(RES)清除、肝脾蓄积毒性及肿瘤微环境异质性进一步限制了ATR纳米药物临床转化。对此,张文丽副教授团队与奥克兰大学Zimei Wu教授团队曾在Advanced Drug Delivery Reviews合作发表相关综述 “Strategies to enhance drug delivery to solid tumors by harnessing the EPR effects and alternative targeting mechanisms”。
为突破ATR瓶颈,本研究构建了四种在肿瘤外基质(ECM)密度,血管分布和EPR效应具有高度异质性的动物模型,并筛选了适合评价ATR转运的动物模型;同时利用高尔基体靶向及抑制内皮顶端侧转运的单向转胞吞跨血管方式,以及穿透细胞外基质,克服连续胞转的肿瘤穿透方式,从完善肿瘤模型和制剂两个角度探索ATR介导的靶向治疗途径;针对EPR效应的非特异性,采用非活性“血小板鬼影”作为纳米制剂的集装箱,凭借其微米尺寸和归巢效应,减少非靶组织的截留,通过调控其膜流动性,实现肿瘤部位纳米载体的级联释放。该研究成功开发了一种基于ATR机制的高效肿瘤靶向系统,为应对肿瘤异质性和开发肿瘤靶向纳米药物提供了新策略。
该研究受到国家留学基金委“促进与加拿大、澳大利亚、新西兰及拉美地区科研合作与高层次人才培养项目”资助。
原文链接:https://doi.org/10.1002/smll.202512807
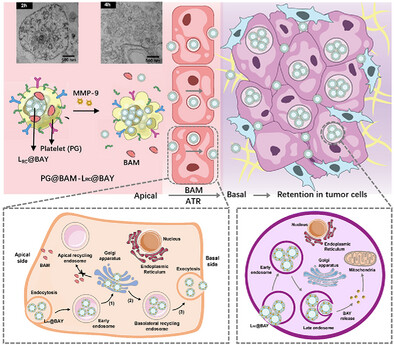
示意图
(供稿单位:药学院,撰写人:刘华)


