脂质异常蓄积是驱动ALD疾病进展的核心因素,却长期缺乏有效靶向治疗策略。传统观念认为CEBPA是促进脂质合成的转录因子,但药学院郝海平/颜婷婷团队与美国国立卫生研究院(NIH)Frank J. Gonzalez团队合作发现:敲除肝细胞CEBPA反而加重了肝脂蓄积与纤维化,并揭示其通过抑制促纤维化靶基因SPP1的转录和分泌参与纤维化调控,然而对肝细胞CEBPA究竟如何抑制肝脂蓄积并调控ALD进展仍知之甚少。
为此,该团队借助以脂质蓄积为主要特征的酒精性肝病小鼠模型并结合临床样本,发现酒精相关性肝炎与肝硬化患者肝脏中CEBPA表达均显著下调,而肝细胞特异性敲除CEBPA会大幅加剧酒精诱导的肝脏脂质堆积—即便在疾病后期敲除,这一表型依然存在。机制研究表明,CEBPA直接激活下游靶基因ORM1的转录,其编码的分泌蛋白ORM1能够结合肝细胞内脂肪酸并促进其外排,从而减轻脂毒性。CEBPA-ORM1信号轴干预实验证实,无论通过基因治疗恢复CEBPA或ORM1表达,还是外源补充重组ORM1蛋白,均可显著缓解ALD相关的肝脏脂质蓄积。该研究首次揭示了CEBPA-ORM1轴抑制ALD进展的新机制,为靶向治疗提供了全新思路,并提示血清ORM1是ALD进展的潜在生物标志物。
该成果成果近日以“Hepatocyte CEBPA-ORM1 axis restricts alcohol-associated liver disease”为题发表在Hepatology期刊。我校药学院赴NIH联合培养博士研究生颜娜娜和NIH夏杨柳博士、张洋博士为该论文的共同第一作者,我校郝海平教授、颜婷婷教授和NIH Frank J. Gonzalez教授为共同通讯作者,中国药科大学为第一通讯单位。本研究受到NIH内部研究基金、国家重大新药创制科技重大专项、国家高层次青年人才计划、国家自然科学基金、江苏省自然科学基金、江苏省双创人才计划、教育部基础与交叉学科突破计划、临港实验室项目、高等学校学科创新引智计划项目及中国药科大学兴药学者计划等资助。
原文链接:https://doi.org/10.1097/HEP.0000000000001737
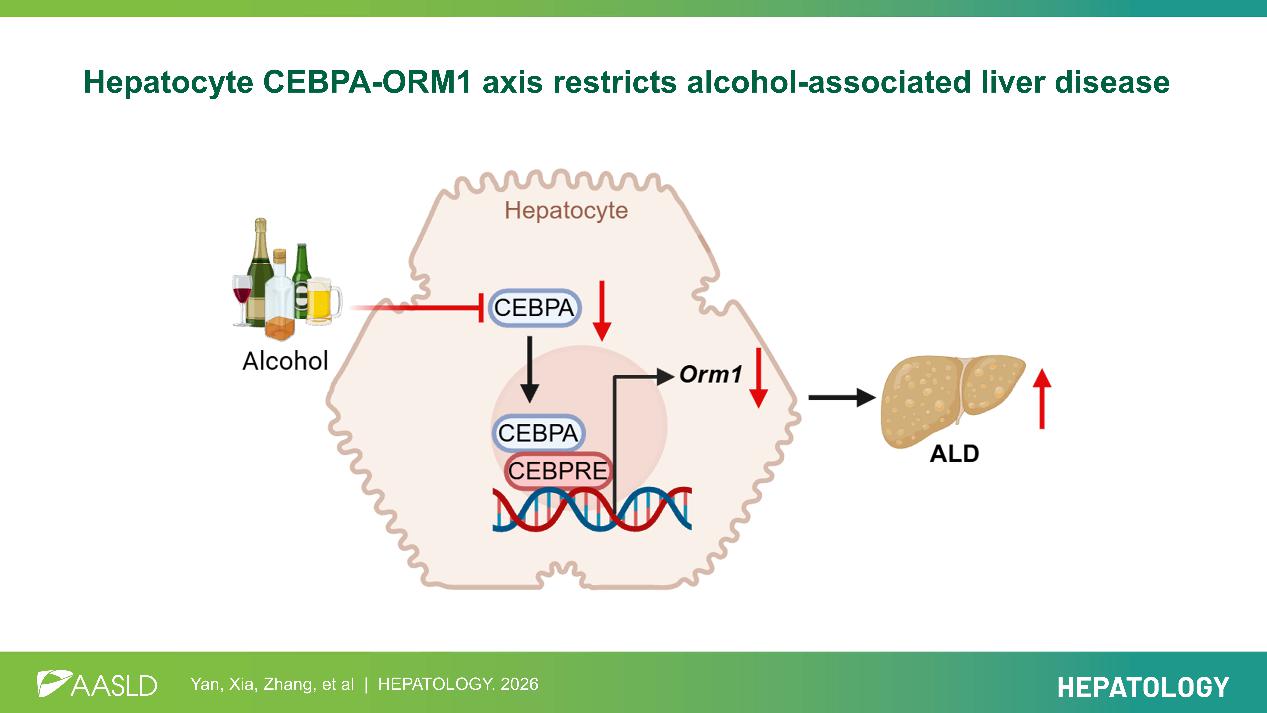
肝细胞CEBPA-ORM1信号轴抑制酒精相关性肝病示意图
(供稿单位:药学院,撰写人:刘华)


