近日,药学院江程教授团队和胡庆华教授团队合作在药物化学领域顶尖期刊Journal of Medicinal Chemistry(IF:8.039)在线发表了最新研究成果:Discovery of a Series of 5-Amide-1H-pyrazole-3-carboxyl Derivatives as Potent P2Y14R Antagonists with Anti-Inflammatory Characters。药学院硕士研究生王雨杭和博士后周梦泽为本论文的共同第一作者,江程教授、胡庆华教授和徐莉莉副研究员为本文的共同通讯作者,中国药科大学为论文的唯一通讯单位。
嘌呤能受体(P2Y)在体内分布广泛,主要被内源性的嘌呤或嘧啶及其糖苷类激活,被认为在多种疾病的发生发展中发挥重要作用。P2Y14受体是P2Y家族中特殊的一员,能够特异性地被UDP-糖苷激活,与机体的免疫调节有着密切的关联。在前期研究中,课题组揭示了P2Y14R在固有免疫细胞死亡中的调节作用,证实了P2Y14R作为急性炎症相关疾病潜在靶标的可行性。然而,目前已有报道的P2Y14受体拮抗剂结构较为单一,其中以高选择性、高活性的PPTN为代表,但PPTN因其极低的溶解度和生物利用度,难以进行进一步的开发。
本研究是在课题组前期工作基础上,采用骨架跃迁的设计策略,设计并合成了一系列5-氨基-1H-吡唑-3-羧酸衍生物。经过对P2Y14受体拮抗剂结构中与受体具有重要作用的基团进行分解,探索适合各个结合区域的优势碎片结构,对优势碎片结构进行整合,获得化合物16。通过筛选表达不同受体的HEK293细胞证实了化合物16对P2Y14受体的高抑制活性和高选择性。为验证设计化合物对P2Y14受体的结合能力,课题组设计并合成了一个P2Y14受体荧光拮抗剂作为探针,通过流式细胞术的方法证明了化合物16具有最强的结合能力。研究表明,所获得的化合物16表现出显著提高的溶解度等理化性质、良好的体内外代谢稳定性和生物利用度等药代动力学特征,具有较优的成药性。经细胞和动物实验验证,化合物16表现出优秀的体内外抗炎活性,可作为候选化合物进行进一步的开发。
本项研究为药物化学学科和药理学学科交叉合作,共同推进。研究工作结果可为新型P2Y14受体拮抗剂的研究提供指导,并为腹膜炎、脓毒血症等炎症疾病提供潜在的治疗药物。
本研究工作得到了国家自然科学基金面上项目(82073685、81773745、81872867和82173675),江苏省海洋药物化合物筛选重点实验室(HY2011902),江苏省“青蓝工程”基金(2632021ZD13)和中央高校基本科研业务费的资助。
论文链接:https://pubs.acs.org/doi/10.1021/acs.jmedchem.2c01632
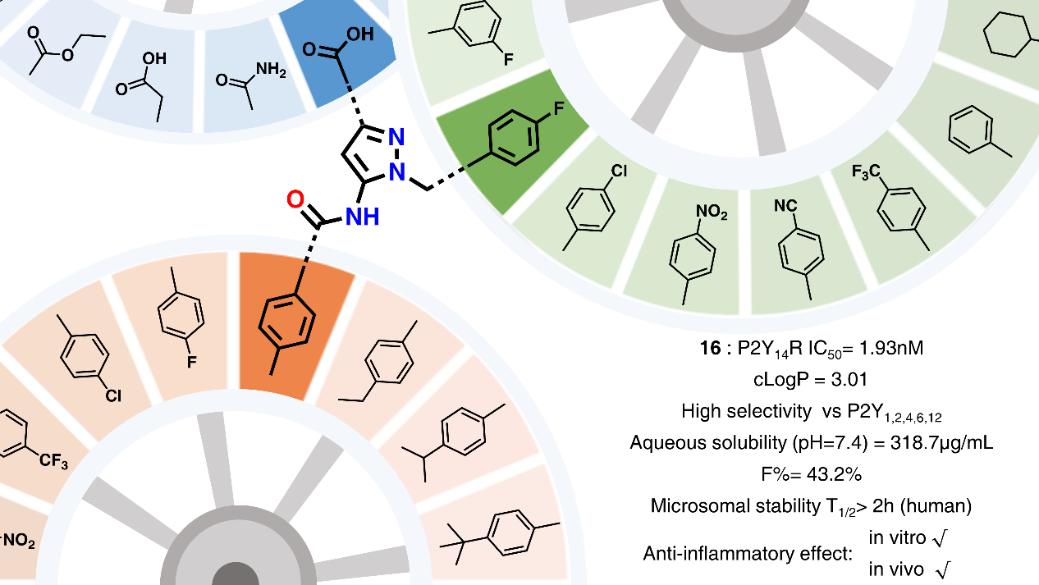
示意图
(供稿单位:药学院,撰写人:刘华)


