2025年第一季度,在学院广大教师的共同努力下,科研成果产出取得了良好成效,以下我们把部分科研成果与大家分享。
01. 董德利/孙志洁团队揭示硝唑尼特有望成为治疗射血分数保留型心衰潜在药物
射血分数保留型心衰(HFpEF)是一种复杂因素相关性疾病,其发生与衰老、肥胖、高血压、糖脂代谢异常以及慢性炎症等因素有关。硝唑尼特(Nitazoxanide)是一种临床抗原虫药物,具有良好的安全性,体内吸收后迅速代谢为替唑尼特(Tizoxanide)发挥药理作用。前期研究发现硝唑尼特及其活性代谢物替唑尼特均具有线粒体解偶联作用,可抑制实验性高脂血症、肝脂肪样变和动脉粥样硬化,改善器官纤维化。基于此,该团队研究了硝唑尼特对HFpEF的影响,发现口服途径给予硝唑尼特可显著抑制高脂饲养联合L-NAME诱导的HFpEF小鼠心肌肥厚、心脏纤维化、心脏舒张功能障碍、心脏脂蓄积、血压升高、运动耐力受损、肝脏脂肪样变、肾纤维化和主动脉收缩功能减退等;揭示了硝唑尼特有望成为治疗HFpEF及相关代谢综合征的潜在药物。
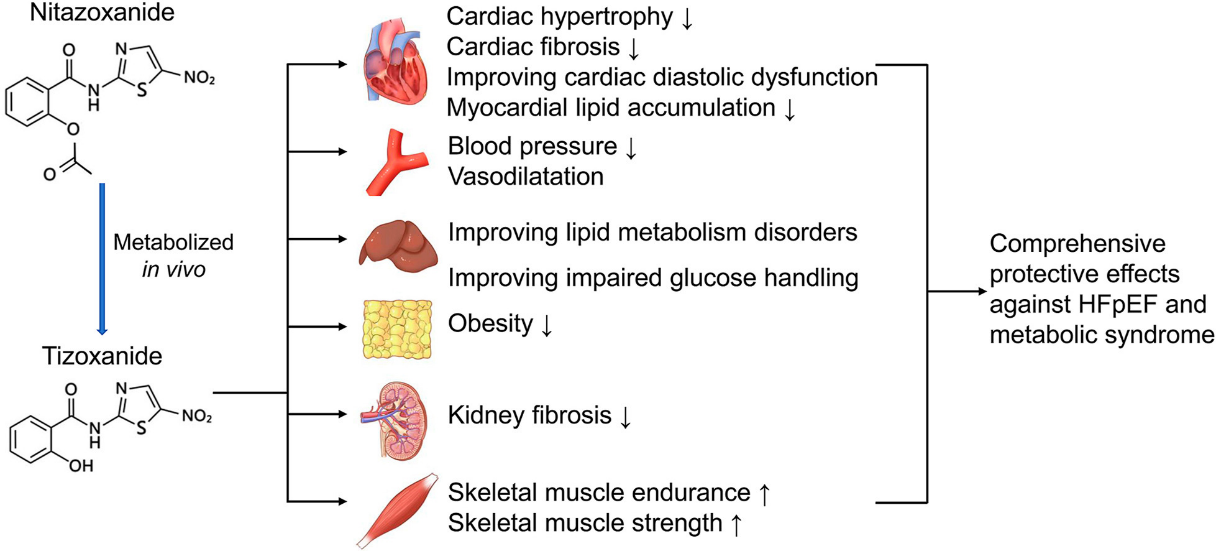
文章信息:Chen J, Zhang L, Xie T, et al. Nitazoxanide protects against heart failure with preserved ejection and metabolic syndrome induced by high-fat diet (HFD) plus L-NAME “two-hit” in mice. Acta Pharmaceutica Sinica B . 2025. https://doi.org/10.1016/j.apsb.2024.12.040
02.王磊/尤启冬团队系统总结2023-2024年间全球首创性药物的突破与进展
首创性药物(First-in-class drug)具备新颖的药物靶点或作用机制,是新药研发的原始驱动力,能为新的药物开发领域和科研方向奠定基础,为相关疾病患者提供全新疗法和卓越疗效。2023-2024年全球首创性药物取得了巨大的成就,小分子药物和大分子药物齐头并进。作者从多个方面分析了首创性药物上市情况、疾病类型、分子类型、靶标类型,全面地展现了首创性药物研发的广阔前景,期待未来医药领域的革新与进步可以为全球公共健康和人类生活质量做出更多的贡献。
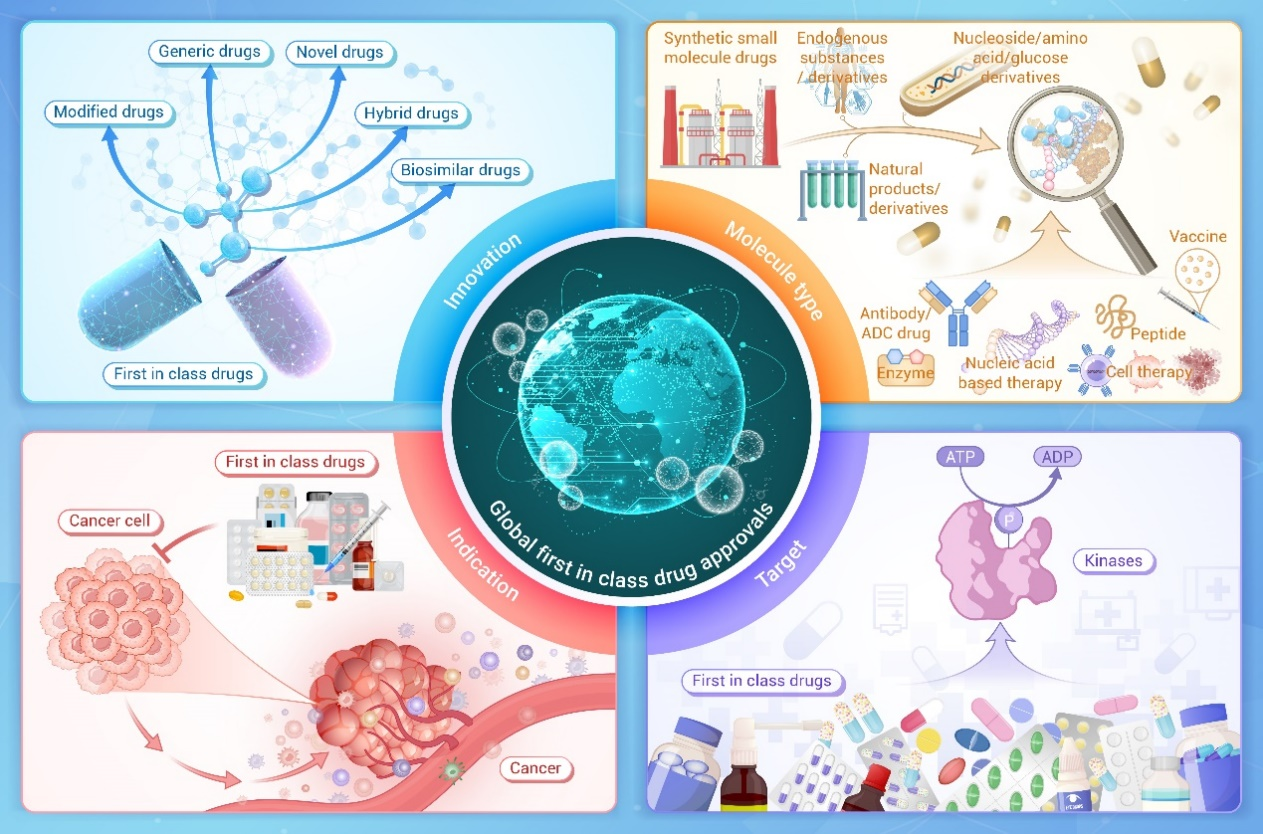
文章信息:Zhai D, Zhang Q, Lu X, et al. Global first-in-class drugs approved in 2023–2024: Breakthroughs and insights. The Innovation. 2025.https://www.cell.com/the-innovation/fulltext/S2666-6758(25)00004-9
03.郝海平团队/熊晶课题组发现调控代谢重塑促进肝再生的新靶标
不同类型肝病成为全球致死致残的重要原因,这是由于肝脏持续受到药物毒物、病毒感染、代谢紊乱、缺血缺氧等致病因素的侵袭。尽管临床有一些针对性的治疗药物,肝损伤患者的生存及恢复大多数情况下仍然依赖于肝脏强大的再生能力。因此,肝再生的机制研究能大大促进肝病新型治疗药物的研发。
研究团队通过整合转录组数据,发现膜转运蛋白SLC13A2是肝大部切除术(PHx)后肝脏再生的关键调节因子。SLC13A2的表达在PHx术后迅速降低,并随着肝脏重量和生理功能的修复而逐渐升高至正常水平。研究团队通过构建肝脏特异性过表达或缺失的小鼠模型,证明SLC13A2促进PHx术及HFD饮食长期喂养造成慢性损伤而诱导的肝再生。机制研究表明:SLC13A2转运柠檬酸,柠檬酸经ACLY催化裂解释放乙酰辅酶A用于胆固醇合成,促进SREBP2活化及胆固醇代谢相关基因(LDLR、HMGCR等)的表达。HMGCR抑制剂洛伐他汀抵消SLC13A2促进的肝脏再生。此外,ACLY抑制剂通过抑制SLC13A2介导的柠檬酸裂解,抑制胆固醇合成,阻遏肝细胞增殖和肝脏再生。研究团队由此提出:由SLC13A2转运的柠檬酸作为中间代谢物恢复肝脏再生的代谢平衡,有望成为减轻肝损伤、促进肝修复的潜在药物靶标。
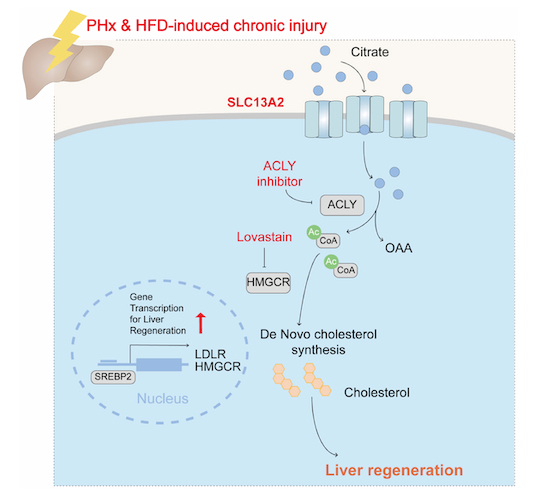
文章信息:Shi L, Chen H, Zhang Y, et al. SLC13A2 promotes hepatocyte metabolic remodeling and liver regeneration by enhancing de novo cholesterol biosynthesis. The EMBO Journal . 2025; 44:1442-1463
04.姜虎林团队开发多功能工程化间充质干细胞用于治疗肺纤维化
肺纤维化是一种进行性疾病,表现为呼吸系统损伤和肺组织功能修复障碍。肺血管生态位通过血管分泌因子在调节肺泡再生中起着至关重要的作用,然而肌成纤维细胞和血管内皮细胞之间的恶性串扰导致纤维化区域肺毛细血管的显著缺失,加剧肺纤维化进程。该团队基于前期干细胞工程化技术,开发了一种多功能工程化间充质干细胞(MSC-MM@LPHN),通过MSC膜表面锚定脂质聚合物纳米粒递送药物诱导肌成纤维细胞去分化,减少内皮细胞损伤因子的分泌,以及抑制血管内皮细胞向纤维化表型转化,从而恢复血管内皮细胞功能;同时结合MSC分泌生长因子促进血管生成作用,重塑纤维化区域正常血管结构,促进肺组织再生并逆转肺纤维化。
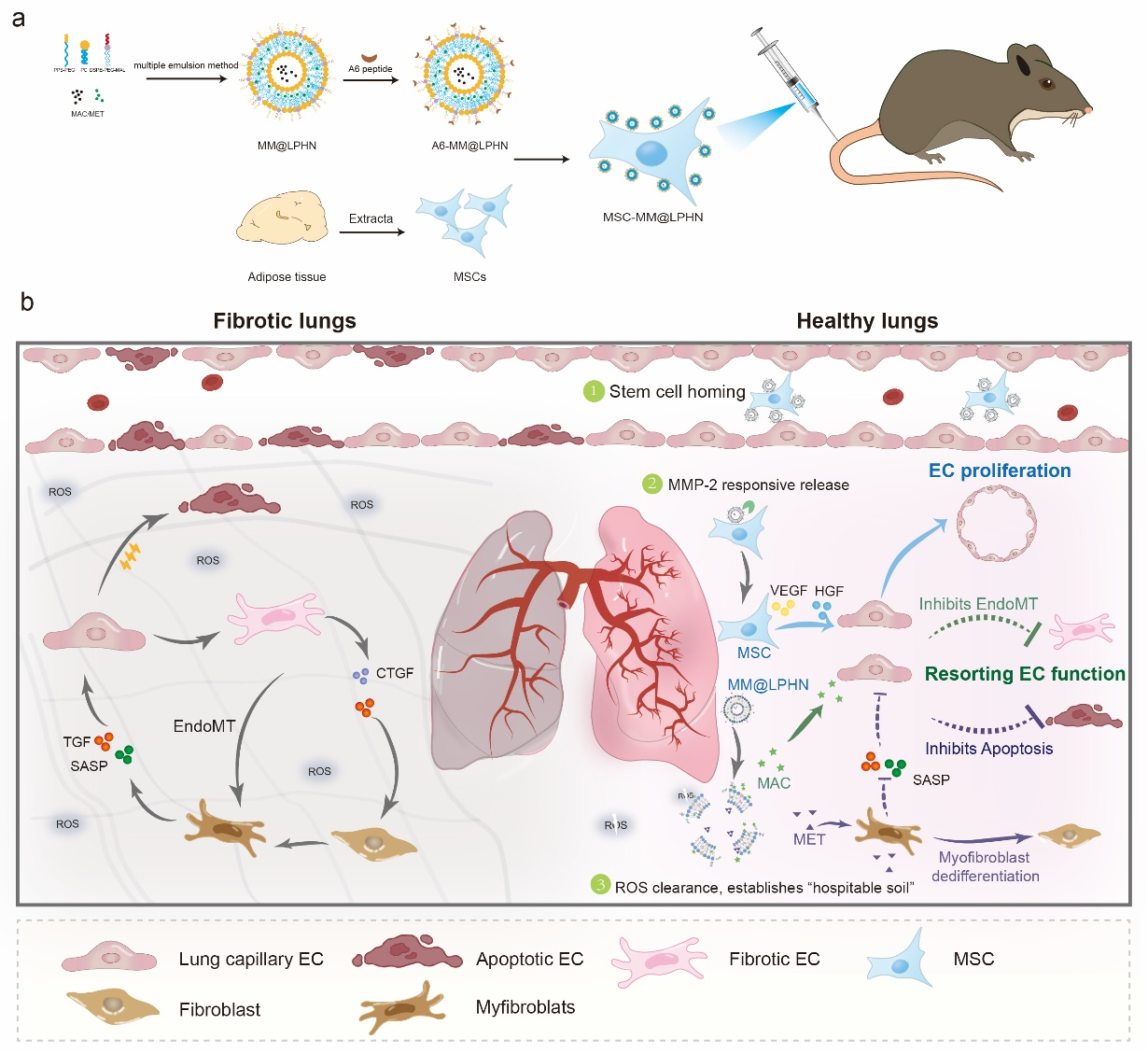
文章信息:Fang Y-F, Zhang C, Han M-M, et al. Engineered MSCs Break Endothelial-Myofibroblast Crosstalk in Pulmonary Fibrosis: Reconstructing the Vascular Niche. Adv. Mater.2025, 2414601
05. 姜虎林团队开发工程化MSC 用于治疗胰腺纤维化
胰腺纤维化是慢性胰腺炎的独特组织病理学特征,表现为正常胰腺实质组织结构丧失,被纤维胶原取代。针对这类以组织修复为病症的疾病,通过具有自我更新、定向分化等功能的干细胞药物进行疾病干预是潜在的治疗手段。该团队前期发现干细胞用于纤维化治疗存在两大挑战:(1)干细胞因其尺寸较大,在纤维胶原层的渗透能力受限,难以定向迁移到病灶深处;(2)纤维化的恶劣微环境造成干细胞在损伤部位迅速凋亡失活,削弱疗效。因此,该团队开发一种一氧化氮脂质体嫁接的工程化MSC,通过调节胶原纤维缓解血管压迫,推动干细胞在胰腺组织分布并增强干细胞体内活性,提高治疗效果。
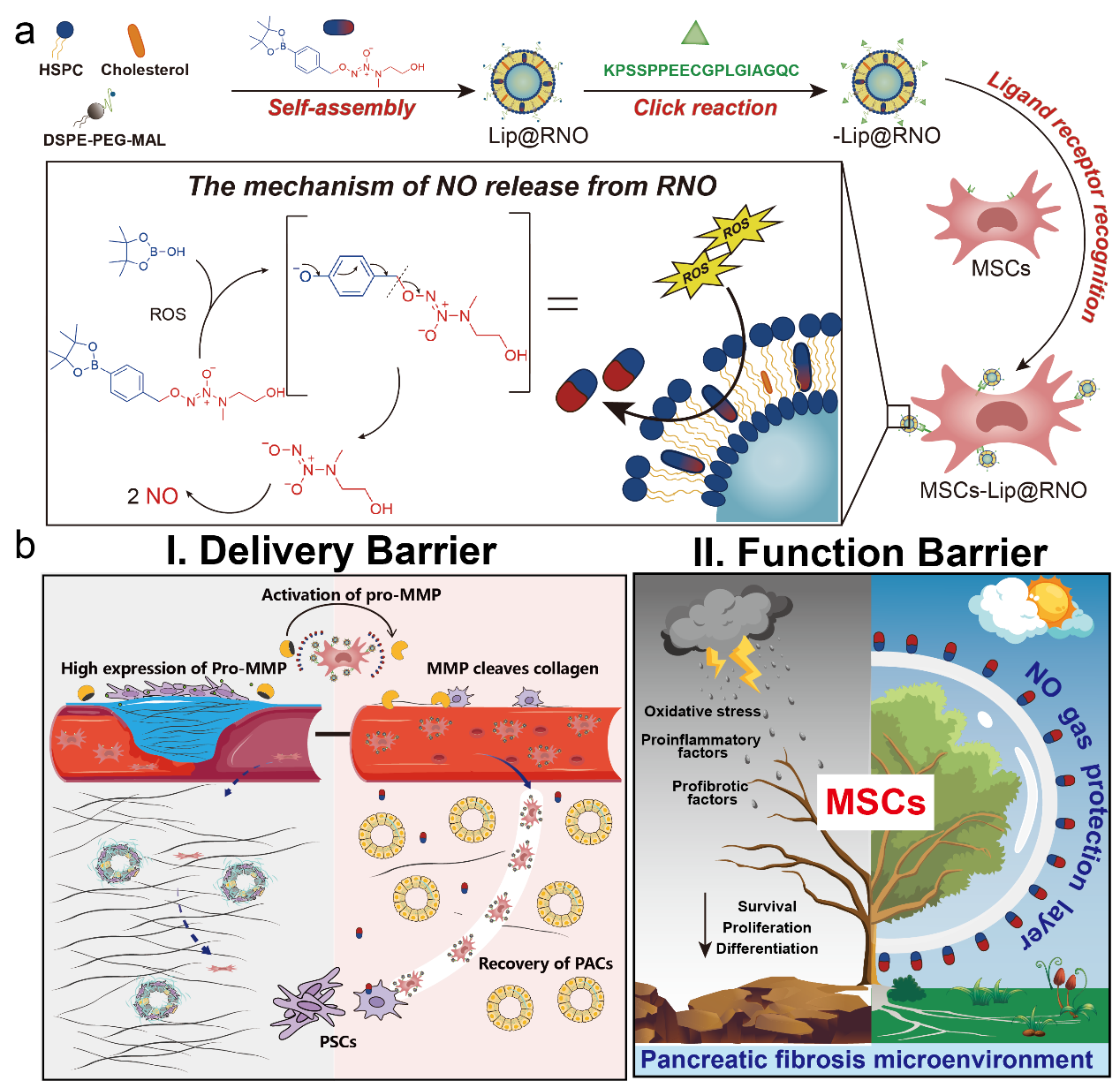
文章信息:Han H, Chen B-T, Liu Y, et al., Engineered Stem Cell Booster Breaks Pathological Barriers to Treat Chronic Pancreatitis. Adv. Mater.2025, 2416261.
06.周建平/丁杨/张华清团队提出利用干细胞转染技术治疗阿尔茨海默病新方法
近年,围绕中枢疾病神经不可逆损伤/丢失难题,基于干细胞的神经再生疗法,通过神经定向分化和细胞网络重建,用于阿尔茨海默病(AD)等诸多神经系统退行性疾病的治疗。但其疗效仍受限于干细胞转染效率不足、细胞存活率低、神经分化难等瓶颈。为解决上述问题,该团队首次提出了一种基于内源载脂蛋白(APOs)的耐血清干细胞转染技术,联合异药双载策略,成功实现了干细胞高效神经分化。为AD等中枢系统疾病治疗提供了新思路和新方案。
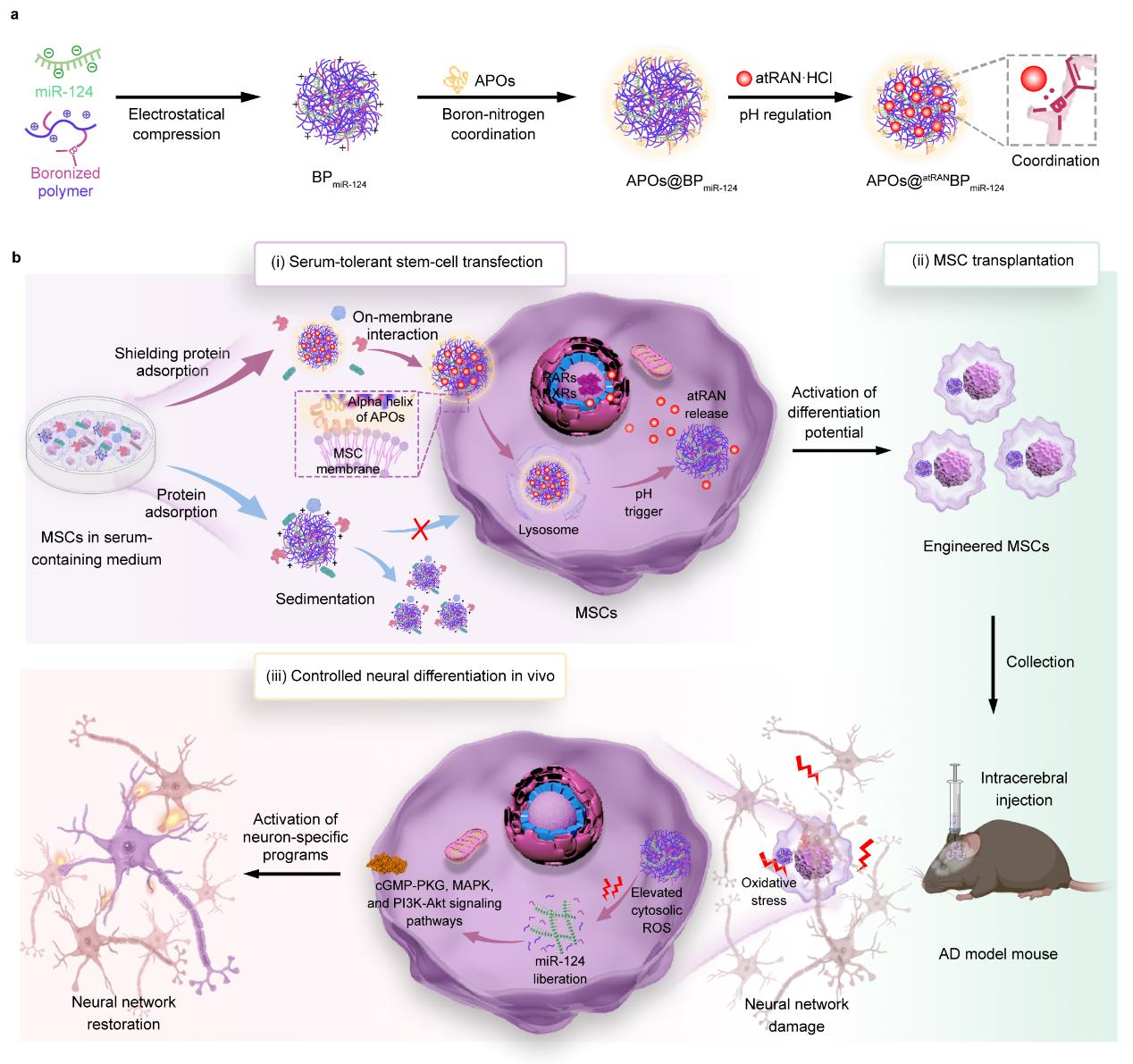
文章信息:
Jin, Y., Han, G., Gao, Y. et al. Serum-tolerant polymeric complex for stem-cell transfection and neural differentiation.Nat.Commun.2025,16,https://doi.org/10.1038/s41467-025-57278-8
07.王磊/尤启冬团队系统总结分子伴侣的生物学作用及其药物靶向策略研究进展
分子伴侣(Molecular chaperone)是一类调节底物蛋白的成熟与翻译后修饰并协助其获得天然构象的蛋白质,对蛋白质稳态的调节起着决定性作用,其中以热休克蛋白家族为主的分子伴侣最为关键,包括small HSPs、HSP40、HSP60、HSP70、HSP90、HSP100及HSP110。近年来,分子伴侣的生物学机制研究及药物靶向策略已取得诸多突破,成为十分有潜力的药物靶标群。
本文系统性回顾该领域30年的发展历程,将靶向分子伴侣系统的小分子药物设计分为四个阶段:(1)HSPs ATPase泛抑制(~1990s);(2)亚型选择性抑制的相关研究(~2000s);(3)靶向分子伴侣系统蛋白互作抑制剂(~2010s);(4)调控分子伴侣系统的多特异性药物设计(~2020s)。着重阐明了四个阶段的分子设计特点,药物发现瓶颈问题,展望了本领域未来药物设计的趋势。
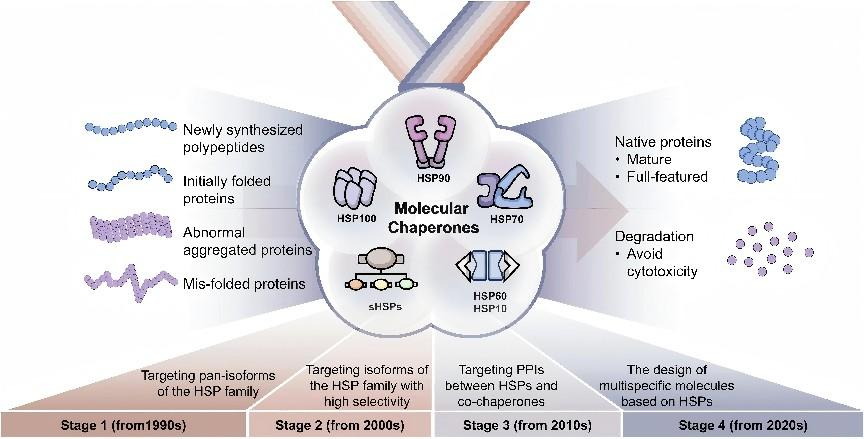
文章信息:Gu, J., He, Y., He, C. et al. Advances in the structures, mechanisms and targeting of molecular chaperones. Sig Transduct Target Ther 10, 84 (2025). https://doi.org/10.1038/s41392-025-02166-2


